(資料圖片僅供參考)
(資料圖片僅供參考)
這種超磷酸化的tau蛋白(或tau低聚物)在癡呆癥患者大腦中的積累導致了神經纖維纏結(NFTs)的產生并最終導致神經元的細胞死亡進而導致該疾病的漸進性神經退行性癥狀。雖然tau蛋白可能被選擇性自噬降解,但其發生的具體機制尚不清楚。
不過來自日本國家量子科學與技術研究所的專家最近進行的研究表明,一個特定的基因--p62基因--在tau齊聚體的選擇性自噬中發揮了關鍵作用。相關研究報告已發表在《Aging Cell》上。
以往的研究報告稱,tau蛋白的異常積累可能通過p62受體蛋白(它是一種選擇性的自噬受體蛋白)被自噬途徑選擇性地抑制。
Maiko Ono指出:“這種蛋白質的泛素結合能力有助于識別有毒的蛋白質聚集物(如tau齊聚體),然后它們可以被細胞過程和細胞器降解。”
然而這項研究的新穎之處在于在一個活體模型中證明了p62的“神經保護 ”作用,這在以前是從未做過的。據悉,他們使用了癡呆癥的小鼠模型。其中一組小鼠的p62基因已被刪除(或敲除),因此它們不表達p62受體蛋白。
在使用免疫染色和比較生物化學分析研究這些小鼠的大腦時,研究人員們發現了一個有趣的情況。在海馬--跟記憶有關的大腦區域--和腦干--協調身體的呼吸、心跳、血壓和其他自愿過程--發現了p62基因敲除(KO)小鼠的神經毒性tau蛋白聚集。當我們考慮到這一點及癡呆癥的癥狀--包括記憶喪失、混亂和情緒變化,這些發現是非常有意義的。
核磁共振掃描顯示,p62 KO小鼠的海馬體已經退化(萎縮)和發炎。對其大腦的尸檢評估顯示其海馬區的神經元損失更大。進一步的免疫熒光研究表明,異常的tau物種聚集可以引起細胞毒性,進而導致p62 KO小鼠的炎癥和神經元的細胞死亡。具體而言,低聚體tau在p62 KO小鼠的大腦中積累更多。
總的來說,這項研究的結果證明,通過消除并因此防止低聚體tau物種在大腦中的聚集,p62在癡呆癥模型中發揮了神經保護作用。
當世界各地的研究人員正在試圖開發治療癡呆癥和其他相關神經退行性疾病的藥物時,這項研究的結果將對提供準確針對tau寡聚物的證據具有重要意義。由于全球老齡人口每年都在增加,因此,開發減緩各種神經退行性疾病的發病和進展的方法的需求也在擴大。這項研究為解決這一需求提供了一個積極的步驟。
-
焦點訊息:隔夜歐美·8月18日
頭條 22-08-18
-
【世界速看料】9部門重磅發文!事關碳達峰碳中和,明確這些目標和任務
頭條 22-08-18
-
天天視點!立方風控鳥·早報(8月18日)
頭條 22-08-18
-
世界熱推薦:盤活1.5萬億元專項債債務限額空間,三季度或為重要窗口期
頭條 22-08-18
-
天天即時看!河南省級農業科技園區增至62家,8000多家企業入駐
頭條 22-08-17
-
世界看點:國家藥監局:《化妝品網絡經營監督管理辦法》公開征求意見
頭條 22-08-17
-
世界百事通!二拍降價7375萬,東興證券4253萬股股票能否售出?
頭條 22-08-17
-
環球快報:雙匯發展:將建設規模化預制菜加工廠,加快布局預制菜產業
頭條 22-08-17
-
焦點速讀:立方風控鳥·晚報(8月17日)
頭條 22-08-17
-
當前觀點:河南召開全省“問題樓盤”破產拯救研討會
頭條 22-08-17
-
天天頭條:“王心凌男孩”救不了芒果超媒,半年上線36檔綜藝業績仍下滑
頭條 22-08-17
-
【天天報資訊】高溫紅色預警繼續發布!7省市部分地區最高氣溫可達40℃以上
頭條 22-08-17
-
焦點熱文:鄭州擬向3.3萬家企業發放失業保險穩崗返還補貼,總計2.45億元
頭條 22-08-17
-
最新消息:營收凈利雙增!安圖生物上半年凈利5.34億元同增29.28%
頭條 22-08-17
-
環球最資訊丨產值目標100億!包頭市發布預制菜產業發展三年行動計劃
頭條 22-08-17
-
環球看點!前7月河南省房地產開發投資4211.70億元,同比下降3.7%
頭條 22-08-17
-
看熱訊:占了全市一半!5個央地合作項目落地鄭州高新區
頭條 22-08-17
-
環球快播:恒星科技上半年營收23.4億元,同比增長37%
頭條 22-08-17
-
今日熱聞!濮耐股份上半年凈利潤1.69億元,同比增長41.76%
頭條 22-08-17
-
信息:河南新增AA+發債平臺,商丘新城建投6億元私募債成功發行
頭條 22-08-17
-
即時:7月全國財政收支情況公布
頭條 22-08-17
-
環球新消息丨日賺逾5億元!三大運營商半年報出爐,擬斥資超500億元大手筆派現
頭條 22-08-17
-
天天觀熱點:南陽:力爭鄧桐、鄭南、南新三條高速年底前開工
頭條 22-08-17
-
天天看點:全國首家!濟南推出二手房“帶押過戶”模式:無須提前還貸、無須墊資
頭條 22-08-17
-
視點!洛陽國宏投資控股集團10億元中票完成發行,利率4.35%
頭條 22-08-17
-
全球快消息!上海市市長、副市長最新工作分工公布
頭條 22-08-17
-
世界訊息:鄭州城建集團5億元私募債完成發行,利率創省內同類債券新低
頭條 22-08-17
-
【時快訊】屠光紹:確實遇到很多困難,但還是要金融開放 | 上海會客廳
頭條 22-08-17
-
全球滾動:合同總額22億元,平頂山市新華區在滬簽約3個項目
頭條 22-08-17
-
【新要聞】以京東云數智能力為企業持續提供產業運營 京東(南陽)數字經濟產業園揭牌
頭條 22-08-17
-
世界最資訊丨哈工大鄭州研究院戰略簽約惠豐鉆石,協助建設金剛石生產線
頭條 22-08-17
-
天天快訊:河南昨日新增本土無癥狀感染者2例
頭條 22-08-17
-
天天速讀:茅臺集團再招751人,應聘科研員需有SCI論文或發明專利
頭條 22-08-17
-
今日播報!隔夜歐美·8月17日
頭條 22-08-17
-
環球短訊!鄭州市政府簽約建設銀行河南省分行,將在高質量發展都市圈等8個領域開展合作
頭條 22-08-17
-
焦點滾動:立方風控鳥·早報(8月17日)
頭條 22-08-17
-
全球快播:皮海洲:中國聯通董事長高喊股價被低估,咋就沒有實際行動呢
頭條 22-08-17
-
全球速遞!鄭州鼓勵企事業單位停車場錯時向市民開放
頭條 22-08-16
-
環球關注:高分紅名單來了!這些公司上半年分紅派現金額超過歸母凈利潤
頭條 22-08-16
-
【全球新要聞】三峽水庫加大下泄向長江中下游補水 未來5天補水約5億立方米
頭條 22-08-16
-
天天熱議:信托業保障基金擬61.52億元受讓華融信托76.79%股權
頭條 22-08-16
-
焦點滾動:立方風控鳥·晚報(8月16日)
頭條 22-08-16
-
世界熱頭條丨總投資60億元,湖北規模最大的光伏電池項目開工
頭條 22-08-16
-
環球快看:?樓陽生在河南省科學院調研
頭條 22-08-16
-
當前快訊:河南省財政下達3.29億元支持公共文化事業高質量發展
頭條 22-08-16
-
最新消息:龍湖集團回應網傳將于8月底破產:謠言,已報案并獲受理
頭條 22-08-16
-
觀察:首日運行平穩 鄭商所組合保證金業務正式上線
頭條 22-08-16
-
環球實時:水利部部署進一步做好長江流域抗旱保供水工作
頭條 22-08-16
-
快播:發布實施辦法,河南建立律師與法官互評機制
頭條 22-08-16
-
觀熱點:新動作!雙匯發展擬成立團餐事業部
頭條 22-08-16
-
世界通訊!全長132公里,嵩縣至內鄉高速公路線路走向公布
頭條 22-08-16
-
【天天報資訊】熱到炸!40℃高溫覆蓋超100萬平方公里,部分地區已現重度氣象干旱
頭條 22-08-16
-
環球快播:雙匯發展上半年凈利潤27.3億元,同比增長7.6%
頭條 22-08-16
-
速遞!快訊!雙匯發展擬成立團餐事業部
頭條 22-08-16
-
【當前獨家】平頂山市人大常委會通過一批人事任免 | 名單
頭條 22-08-16
- 每日消息!新研究發現蛋白質p62有助于預防老2022-08-18
- 世界快看:歐空局拍攝到壯觀的星系“舞蹈”2022-08-18
- 如何解決塑料袋“超重”陰陽價等問題 市場2022-08-18
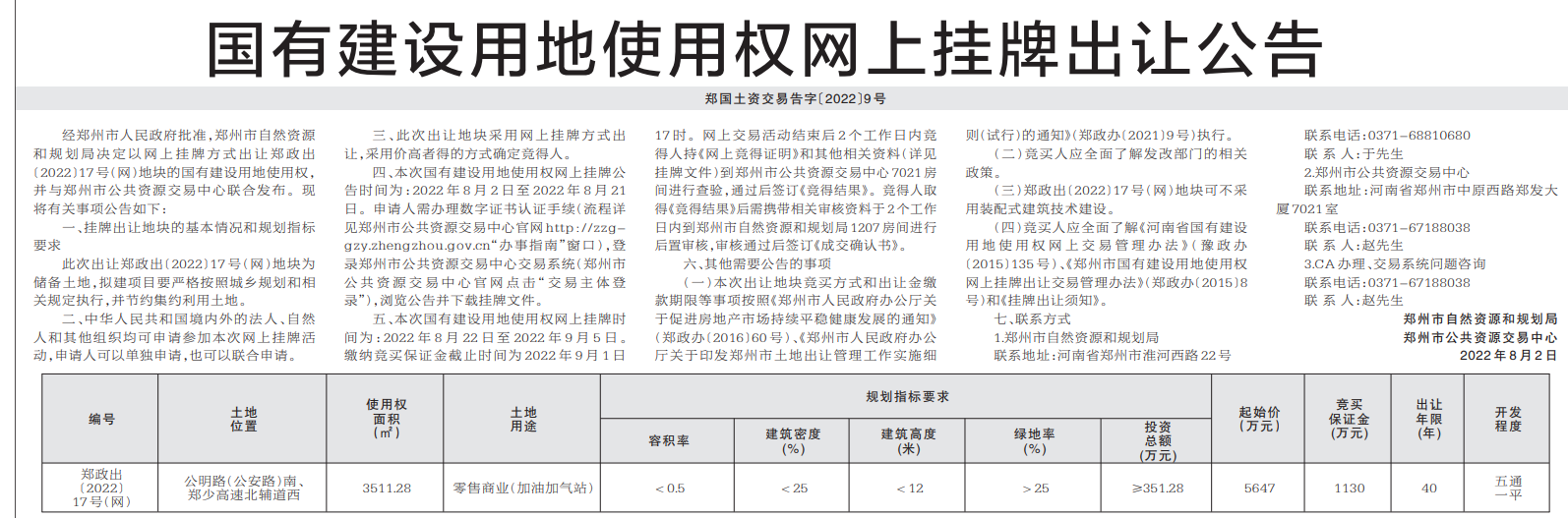
- 鄭州17宗用地集中掛牌總起價超126億 將于92022-08-18
- 鄭州616輛渣土車“升級”新能源 17家渣土2022-08-18
- 8月預計13個樓盤項目扎堆入市 鄭州樓市或2022-08-18
- 8月預計13個樓盤項目扎堆入市 鄭州樓市或2022-08-18
- 河南省7月份經濟運行“成績單”出爐 總體2022-08-18
- “萬人助萬企 金秋招聘月”專場招聘會來啦2022-08-18
- 臺輝高速濮陽清豐段鄭州至濟南鐵路上跨施工2022-08-18
- 18日起鄭州市這個路段老舊供熱管網開始改造2022-08-18
- 河南交警曬出“百日行動”半程成績單 累計2022-08-18
- 河南省促進體育產業高質量發展行動方案公布2022-08-18
- 第九批河南省農業科技園區名單公布 河南省2022-08-18
- 河南省前7個月技術合同成交額達到620.78億2022-08-18
- 今明兩天河南中南部37℃+高溫悶熱天氣南部2022-08-18
- 河南特崗教師筆試成績面試名單公布時間看這2022-08-18
- 請儲水!8月18日起鄭州這些區域將要停水!2022-08-18
- 鄭州發布135號通告:所有高中風險區全部解2022-08-18
- 鄭州公積金線上提取更方便(內附操作指南)2022-08-18
- 全球動態:創業“明星”楊健:當大米遇上高2022-08-18
- 焦點資訊:多地電力吃緊 專家:極端天氣所2022-08-18
- 天天觀天下!北京昨日新增4例本土確診病例2022-08-18
- 鄭州市區小學入學現場報名將于21日至22日進2022-08-18
- 焦點訊息:隔夜歐美·8月18日2022-08-18
- 【世界速看料】9部門重磅發文!事關碳達峰2022-08-18
- 天天視點!立方風控鳥·早報(8月18日)2022-08-18
- 每日快看:2022年8月18日06時空氣污染氣象2022-08-18
- 最新消息:2022年8月18日06時商丘市短期天2022-08-18
- 鄭州首小時免費停車場最全名單 一定要快快2022-08-18
精彩推薦
閱讀排行
- 河南省7月份經濟運行“成績單”出爐 總體持續恢復有所企穩
- 河南交警曬出“百日行動”半程成績單 累計查處公路交通違法行為13萬起
- 河南省促進體育產業高質量發展行動方案公布 到2025年體育產業總規模超過2500億元
- 第九批河南省農業科技園區名單公布 河南省級農業科技園區增至62家
- 河南省前7個月技術合同成交額達到620.78億元 超去年全年
- 河南特崗教師筆試成績面試名單公布時間看這里
- 簡訊:2022河南省央地合作“云簽約”活動舉行 這兩項合作為河南發展注入“數字力量”
- 【天天快播報】因存在各種環境突出問題,河南這11家企業被降級!
- 天天簡訊:河南文旅元宇宙創造者大賽全攻略來了,百萬獎金等你來!
- 全球頭條:軍事動作爽片《狼群》定檔中秋,張晉李治廷“對戰”恐怖組織