前天,美國食品和藥物管理局(FDA)宣布批準(zhǔn)Aduhelm(aducanumab)用于治療早期阿爾茨海默病患者的生物制品許可(BLA)申請(qǐng)。
“阿爾茨海默病是一種毀滅性疾病,會(huì)對(duì)被診斷出患有這種疾病的人及其親人的生活產(chǎn)生深遠(yuǎn)的影響,”FDA藥物評(píng)價(jià)和研究中心主任、醫(yī)學(xué)博士Patrizia Cavazzoni說,“目前可用的療法只能治療疾病的癥狀;這種治療方案是第一種針對(duì)阿爾茨海默病的潛在疾病過程并對(duì)其產(chǎn)生影響的療法。正如我們從抗癌斗爭(zhēng)中了解到的那樣,加速審批途徑可以更快地為患者帶來治療方法,同時(shí)刺激更多的研究和創(chuàng)新。”
FDA在公告中稱,阿爾茨海默病是一種不可逆轉(zhuǎn)的漸進(jìn)性腦部疾病,它會(huì)慢慢破壞記憶和思維能力,并最終破壞執(zhí)行簡(jiǎn)單任務(wù)的能力。
雖然阿爾茨海默病的具體原因尚不完全清楚,但它的特點(diǎn)是大腦的變化——包括淀粉樣斑塊和神經(jīng)原纖維或tau纏結(jié)——導(dǎo)致神經(jīng)元及其連接的喪失。這些變化會(huì)影響一個(gè)人的記憶和思考能力。
Aduhelm(aducanumab)是自2003年以來FDA批準(zhǔn)的首個(gè)治療AD(阿爾茨海默病)的新藥,也是首個(gè)針對(duì)該疾病基本病理生理學(xué)的療法。
此次Aduhelm(aducanumab)是有條件上市,根據(jù)加速批準(zhǔn)條款,F(xiàn)DA要求Biogen公司進(jìn)行一項(xiàng)新的隨機(jī)對(duì)照臨床試驗(yàn),以驗(yàn)證該藥物的臨床益處。如果試驗(yàn)未能驗(yàn)證臨床獲益,F(xiàn)DA 可能會(huì)啟動(dòng)程序以撤回對(duì)該藥物的批準(zhǔn)。
Aduhelm(aducanumab)獲批上市,對(duì)阿爾茨海默病的治療能帶來哪些作用?快報(bào)記者采訪了相關(guān)臨床專家。
浙江大學(xué)醫(yī)學(xué)院附屬邵逸夫醫(yī)院精神衛(wèi)生科主任陳煒教授表示,阿爾茨海默病是困擾全世界醫(yī)生的一大難題,到現(xiàn)在為止,沒有任何一款藥可以阻止疾病的進(jìn)展。“Aduhelm(aducanumab)獲批上市,是大家期待已久的,作為一款治療AD的修飾性藥物,從理論上說,可以使病因得到控制,從而阻止疾病進(jìn)展。”
但陳煒教授也坦言,這款新藥是有條件批準(zhǔn)上市,療效還需要更多臨床數(shù)據(jù)支撐。“從前期臨床研究看,兩個(gè)試驗(yàn)的結(jié)果有很大的不同,提示這款藥可能對(duì)部分患者有效,那么具體哪類患者有效還需要進(jìn)一步分析。此外,抗淀粉樣蛋白類藥物可能會(huì)引起一些副反應(yīng),比如腦細(xì)胞水腫,如何平衡療效和不良反應(yīng),需要臨床醫(yī)生進(jìn)一步觀察。”
“任何一款新藥的上市、臨床應(yīng)用,安全性始終是第一位,在保證安全的前提下,然后再來講療效。” 陳煒教授說。
浙江大學(xué)醫(yī)學(xué)院附屬精神衛(wèi)生中心(杭州市第七人民醫(yī)院)老年精神大科主任陳斌華也表示,治療阿爾茨海默病的新藥上市,這是個(gè)好消息。“從藥物的作用途徑看,理論上來講,因?yàn)槭强贵w類藥物,直接作用于β淀粉樣蛋白,針對(duì)性更強(qiáng),作為醫(yī)生還是蠻期待它的臨床表現(xiàn)的。”
Aducanumab是一種高親和力、靶向- Aβ構(gòu)象表位的全人IgG1單克隆抗體。它能夠有選擇性地與AD患者大腦中的淀粉樣蛋白沉積結(jié)合,然后通過激活免疫系統(tǒng),將大腦中的沉積蛋白清除。
對(duì)此,陳斌華主任提到,作為生物制品免疫療法,副反應(yīng)方面要特別關(guān)注。“以前就有幾種免疫療法新藥,在臨床研究或動(dòng)物實(shí)驗(yàn)階段,因?yàn)槌霈F(xiàn)腦水腫等嚴(yán)重免疫反應(yīng),不得不中止實(shí)驗(yàn)。”
此外,過敏反應(yīng)也是要關(guān)注的問題,“生物制品作用于人體,如果對(duì)抗體產(chǎn)生免疫應(yīng)答,出現(xiàn)嚴(yán)重的過敏反應(yīng),就可能損傷身體臟器。”
陳斌華表示, “雖然這款藥的上市之路頗為波折,也很有爭(zhēng)議,但在沒有特效藥的當(dāng)下,新藥獲批上市,或許能給患者、家屬、醫(yī)生都帶來一些希望。對(duì)于一個(gè)新藥的評(píng)價(jià),我們不僅僅要看實(shí)驗(yàn)室的研究數(shù)據(jù),更需要通過時(shí)間去驗(yàn)證綜合狀態(tài)下的臨床應(yīng)用。”(記者 金晶 通訊員 王家鈴 李文芳 李彬)
-
深圳一男子加油站拔油槍點(diǎn)燃后逃跑 警方已介入調(diào)查縱火人員已鎖定
頭條 21-12-17
-
淚目!95歲媽媽病床前親吻74歲生病的女兒 網(wǎng)友:孩子不管多大都是媽媽的寶貝
頭條 21-12-15
-
川妹子抽中50顆榴蓮直呼吃不完!網(wǎng)友:可以共享你的負(fù)擔(dān)嗎?
頭條 21-12-15
-
河南省政府發(fā)布2022年元旦放假通知
頭條 21-12-15
-
濮陽市聚碳新材料產(chǎn)業(yè)聯(lián)盟成立
頭條 21-12-15
-
預(yù)計(jì)明年超50家企業(yè)回歸,瑞銀稱中概股H股上市將繼續(xù)升溫
頭條 21-12-15
-
新鄉(xiāng)發(fā)現(xiàn)一境外輸入奧密克戎病例密接者,活動(dòng)軌跡公布
頭條 21-12-15
-
河南:中藥配方顆粒不得在醫(yī)療機(jī)構(gòu)以外銷售
頭條 21-12-15
-
中原環(huán)保完成發(fā)行5億元超短融,利率2.95%
頭條 21-12-15
-
南陽市政府將與中車四方所在新能源裝備等領(lǐng)域開展深入合作
頭條 21-12-15
-
鄭州出臺(tái)新措施:公租房可“掌上”繳租秒辦理
頭條 21-12-15
-
國家統(tǒng)計(jì)局:11月社會(huì)消費(fèi)品零售總額增長3.9%
頭條 21-12-15
-
中國11月規(guī)上工業(yè)增加值同比增長3.8%
頭條 21-12-15
-
1207萬!全年就業(yè)超額完成預(yù)期目標(biāo)
頭條 21-12-15
-
河南凱旺科技公開發(fā)行2396萬股新股,獲6321.47倍申購
頭條 21-12-15
-
隔夜歐美·12月15日
頭條 21-12-15
-
多部委密集部署明年工作!三大看點(diǎn)值得關(guān)注
頭條 21-12-15
-
立方風(fēng)控鳥·早報(bào)(12月15日)
頭條 21-12-15
-
醫(yī)藥巨頭今日登陸科創(chuàng)板!高瓴重倉"陪伴",引入"綠鞋"機(jī)制
頭條 21-12-15
-
皮海洲:臨門一腳踏剎車!龍竹科技終止轉(zhuǎn)板說明了什么
頭條 21-12-15
-
立方風(fēng)控鳥·晚報(bào)(12月14日)
頭條 21-12-14
-
總投資額超百億!中建七局接連中標(biāo)兩個(gè)EPC總承包項(xiàng)目
頭條 21-12-14
-
信陽華信投資集團(tuán)10億元中票完成發(fā)行,利率3.70%
頭條 21-12-14
-
新強(qiáng)聯(lián)擬擇機(jī)出售所持明陽智能股票
頭條 21-12-14
-
洛陽新強(qiáng)聯(lián)擬億元入股山東擬IPO公司,持股4.50%
頭條 21-12-14
-
河南7種輕微交通違法可免罰
頭條 21-12-14
-
浙江樂清民警自曝37歲未婚救下輕生女子 網(wǎng)友:一定要最愛自己
頭條 21-12-14
-
女子9樓墜落緊緊抓住7樓防護(hù)窗所幸有驚無險(xiǎn)!網(wǎng)友:不幸中的萬幸啊
頭條 21-12-07
-
江西一年級(jí)萌娃穿航天服走方陣 網(wǎng)友:可可愛愛的小小航天員
頭條 21-12-06
-
女子精心養(yǎng)了半年的盆栽竟是塑料做的 網(wǎng)友:這是做的有多真
頭條 21-11-30
-
河南鄭州一女子懷上八胞胎!醫(yī)生一句話說出罕見原因 全家又喜又憂
頭條 21-11-26
-
神奇!女子用砂鍋煮綠豆粥自動(dòng)吐皮 網(wǎng)友:這個(gè)鍋好“懂事”
頭條 21-11-23
-
湖南一懷孕老師暈倒學(xué)生們立刻化身“閃電俠”飛奔相救
頭條 21-11-23
-
26歲癌癥女孩刷單被騙23萬救命錢 想掙外快結(jié)果救命錢打了水漂
頭條 21-11-23
-
男子撿槍上交進(jìn)門瞬間嚇壞警察迅速拔槍警戒 網(wǎng)友:進(jìn)門倒是說一聲啊
頭條 21-11-19
-
硬核!男子酒后執(zhí)意開車被兄弟卸掉輪胎 網(wǎng)友:這才是真朋友啊!
頭條 21-11-18
-
撒貝寧時(shí)隔4年回歸主持今日說法 網(wǎng)友激動(dòng)喊話:“爺青回”
頭條 21-11-18
-
廣州一流浪貓被五星級(jí)酒店收留憑實(shí)力找到長期飯票 每天吃米其林星級(jí)員工餐
頭條 21-11-17
-
經(jīng)商奇才!長春女子為南方人雪地代寫6天賺300元 網(wǎng)友:雪起碼得分三成
頭條 21-11-16
-
實(shí)用又好看!陜西渭南村民在院墻上栽滿仙人掌防盜 網(wǎng)友:真的很好看~
頭條 21-11-15
-
果農(nóng)“為國家做研究”捐橘子 網(wǎng)店老板找到了!老板:大家理性消費(fèi)
頭條 21-11-15
- 《南京市中小學(xué)生營養(yǎng)午餐指南》(2021版)2021-12-20
- “十四五”我國將大力提高技工待遇 推動(dòng)高2021-12-20
- 修訂后的《高等學(xué)校思想政治理論課建設(shè)標(biāo)準(zhǔn)2021-12-20
- 內(nèi)地奧運(yùn)健兒與澳門青少年運(yùn)動(dòng)員開展對(duì)話交2021-12-20
- 香港中聯(lián)辦聲明:祝賀香港特區(qū)第七屆立法會(huì)2021-12-20
- 今日起 石家莊市區(qū)小學(xué)生和幼兒上下學(xué)免費(fèi)2021-12-20
- 江西南昌殺妻拋尸案二審維持死刑:被告人主2021-12-20
- 山東通報(bào)關(guān)于藝考考生違規(guī)攜帶手機(jī)網(wǎng)傳試卷2021-12-20
- 戰(zhàn)鼓催征練兵急——第81集團(tuán)軍某旅學(xué)習(xí)十九2021-12-20
- “十四五”縣域普通高中發(fā)展提升行動(dòng)計(jì)劃 2021-12-20
- 《全國普通高校本科教育教學(xué)質(zhì)量報(bào)告(20202021-12-20
- “中小學(xué)教師的負(fù)擔(dān)也要真的減下來” 教師2021-12-20
- 鄭濟(jì)高鐵鄭濮段首個(gè)動(dòng)力“心臟”送電 其他2021-12-20
- 河南印發(fā)緊急通知 即日起至明年2月底開展2021-12-20
- 降溫!暴雪!本周河南氣溫將出現(xiàn)今年入冬以2021-12-20
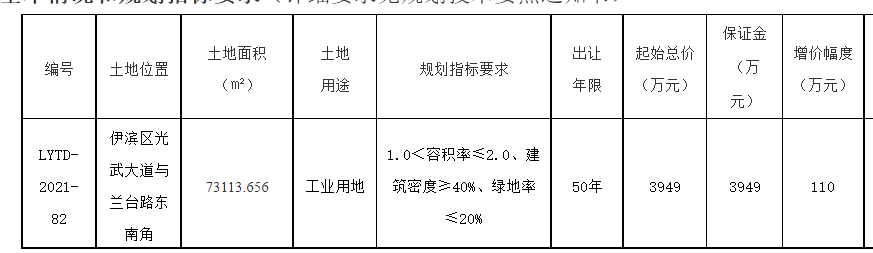
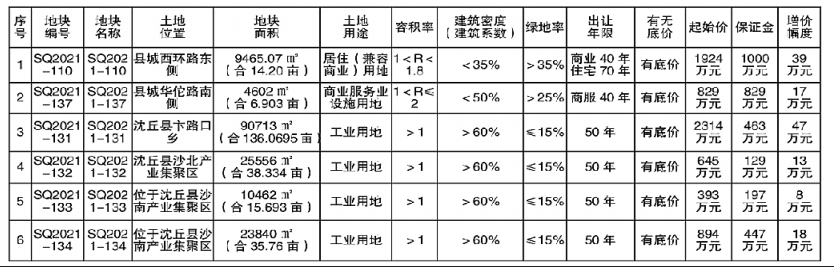
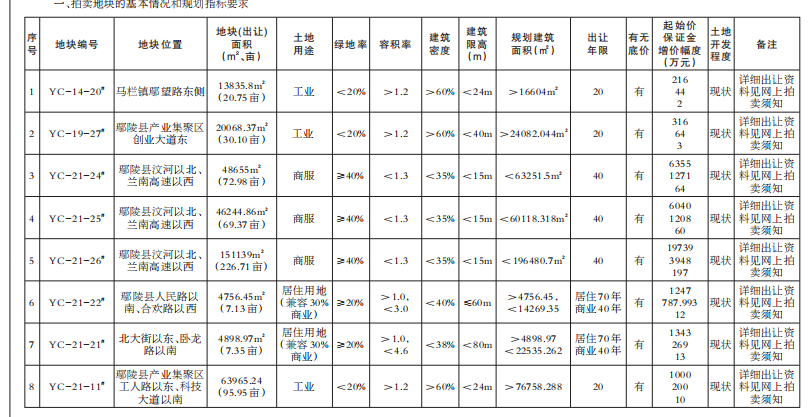
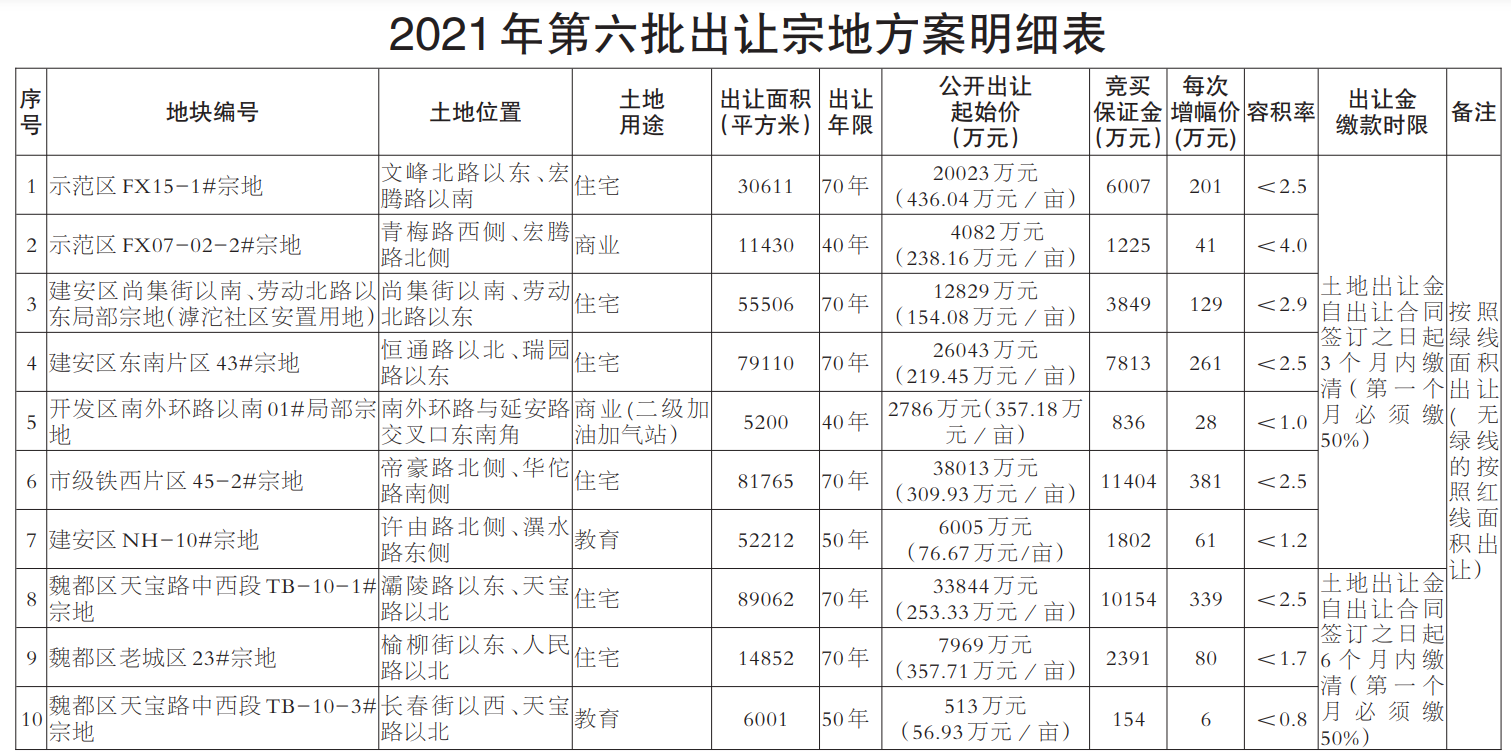
- 綠維文旅:土地開發(fā)與運(yùn)營要點(diǎn)2021-12-20
- 顛覆級(jí)豪華改裝登場(chǎng),風(fēng)行M7領(lǐng)爵款演繹豪華2021-12-20
- 借力清華大學(xué)課題研究 顧家家居與高校年輕2021-12-20
- 14萬起售即豪華,進(jìn)階MPV世家煥新力作東風(fēng)2021-12-20
- 周口小學(xué)生被校長拍打頭部后病發(fā) 校長是否2021-12-20
- 太揪心!山西孝義透水事故獲救人員講述被困2021-12-20
- 國家衛(wèi)健委:昨日新增本土確診病例37例,其2021-12-20
- 浙江省新增確診病例12例,其中杭州市1例、2021-12-20
- 浙江昨日新增本土確診病例10例 境外輸入確2021-12-20
- 內(nèi)蒙古昨日新增境外輸入確診病例7例2021-12-20
- 香港特區(qū)政府新聞公報(bào):行政長官林鄭月娥將2021-12-20
- 河南高純石英砂提純技術(shù)獲突破 提純二氧化2021-12-20
- 鄭州一年內(nèi)新增易貨公司100多家 靠收服務(wù)2021-12-20
- 出山店水庫移民安置工作通過國家驗(yàn)收 歷時(shí)2021-12-20
- 鶴壁辛村遺址發(fā)現(xiàn)殷遺民貴族墓葬2021-12-20
精彩推薦
閱讀排行
- 降溫!暴雪!本周河南氣溫將出現(xiàn)今年入冬以來最低值 最高氣溫降至0~2℃
- 河南高純石英砂提純技術(shù)獲突破 提純二氧化硅純度達(dá)到了99.998%
- 鶴壁辛村遺址發(fā)現(xiàn)殷遺民貴族墓葬
- 河南省《通知》 確定175家企業(yè)為知識(shí)產(chǎn)權(quán)強(qiáng)企
- 河南出臺(tái)《方案》 到2025年公民具備科學(xué)素質(zhì)比例將超15%
- 11月份河南全省經(jīng)濟(jì)運(yùn)行情況發(fā)布 新興動(dòng)能持續(xù)增強(qiáng)經(jīng)濟(jì)運(yùn)行延續(xù)恢復(fù)態(tài)勢(shì)
- 提醒!河南省2021年度文物勘探許可證年審工作啟動(dòng)
- 河南提前完成惠民惠農(nóng)財(cái)政補(bǔ)貼資金“一卡通”管理全年目標(biāo)
- 河南發(fā)文加快補(bǔ)齊全民健身場(chǎng)地設(shè)施短板 探索“體育+公園”新模式
- 2021年度河南省體育產(chǎn)業(yè)示范單位示范項(xiàng)目評(píng)選結(jié)果公示